近日,我校刘三宏和海军军医大学张卫东团队在Acta Pharmaceutica Sinica B发表去甲泽拉木醛通过靶向USP22降解PD-L1发挥免疫抗肿瘤方面的最新研究成果Demethylzeylasteral induces PD-L1 ubiquitin-proteasome degradation and promotes antitumor immunity via targeting USP22。

近年来,肿瘤免疫疗法的崛起已成为继手术、放疗、化疗和靶向治疗之后的另一种重要的临床治疗手段。尤其是针对免疫检查点如PD-1/PD-L1和CTLA-4的抗体治疗,已在临床上显示出显著疗效。然而,这些抗体药物的应用也面临一些挑战,包括患者响应率有限和可能引发的免疫相关不良事件。为了克服这些限制,研究者们正在探索新的治疗策略,以期提升肿瘤免疫疗法的效果并减少其副作用。小分子药物因其独特的特性,在肿瘤免疫治疗中显示出巨大潜力。与抗体药物相比,小分子药物具有以下优势:更高的口服生物利用度、更低的生产和管理成本、更强的肿瘤环境渗透性,以及能够穿透细胞膜并作用于细胞内靶点。此外,小分子药物较短的半衰期也降低了它们引发长期不良反应的风险。因此,基于小分子药物的治疗策略正在肿瘤免疫治疗领域受到越来越多的关注。
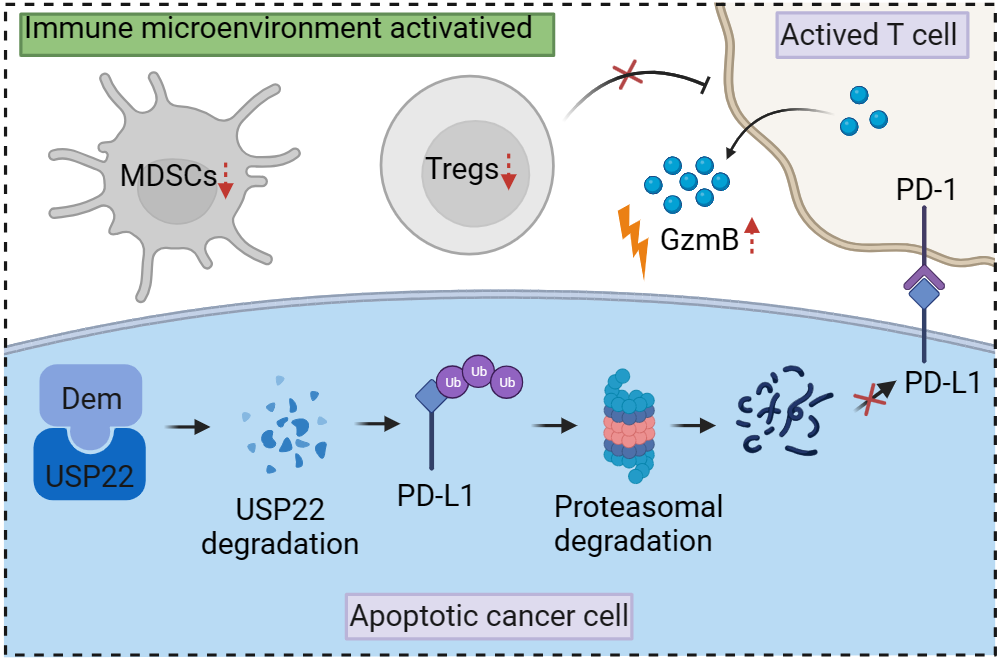
我校刘三宏和海军军医大学张卫东课题组长期致力于从天然活性产物中寻找作用机制新颖的肿瘤免疫治疗小分子药物。研究人员从一个包含225个中药小分子的化合物库中发现去甲泽拉木醛(Dem)可以显著下调结直肠癌细胞中PD-L1的表达,并增强T细胞对肿瘤细胞的杀伤作用。机制研究表明,Dem与去泛素化酶USP22结合并促进其降解,从而增加PD-L1的泛素化并通过蛋白酶体途径引起其降解。此外,Dem增加了细胞毒性T细胞的活性,减少了肿瘤浸润淋巴细胞(TILs)中髓源性抑制细胞(MDSCs)和调节性T细胞(Tregs)的数量,从而激活了C57BL/6小鼠的肿瘤免疫微环境并抑制了皮下移植瘤的生长。研究还发现Dem和CTLA-4抗体的组合可以进一步提高抗肿瘤治疗的疗效。该研究揭示了Dem促进PD-L1降解的机制,并表明Dem和CTLA-4抗体的联合可能提高免疫治疗的疗效。这项创新性研究为Dem作为潜在的肿瘤免疫治疗小分子药物的开发提供了坚实的科学基础。
上海中医药大学硕士研究生张炎炎和黄昀为论文共同第一作者,张卫东教授、刘三宏研究员和王群副研究员为共同通讯作者。该研究得到国家自然科学基金、国家中医药管理局创新团队项目和上海市中药化学生物学前沿研究基地项目的资助支持。(科技处)


